Giáo án ôn tập Hóa học Lớp 8 - Tuần 22, Bài 28: Không khí. Sự cháy. Bài luyện tập 5 - Lê Duy Minh
Bạn đang xem tài liệu "Giáo án ôn tập Hóa học Lớp 8 - Tuần 22, Bài 28: Không khí. Sự cháy. Bài luyện tập 5 - Lê Duy Minh", để tải tài liệu gốc về máy hãy click vào nút Download ở trên.
Tóm tắt nội dung tài liệu: Giáo án ôn tập Hóa học Lớp 8 - Tuần 22, Bài 28: Không khí. Sự cháy. Bài luyện tập 5 - Lê Duy Minh
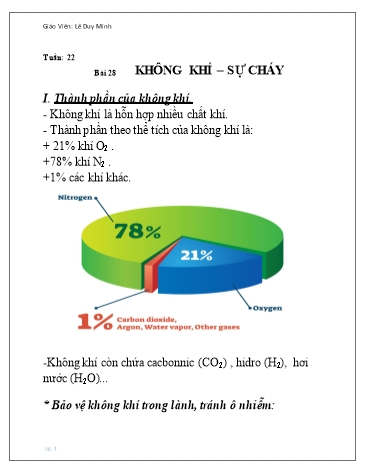
Giáo Viên: Lê Duy Minh Tuần: 22 Bài 28 KHÔNG KHÍ – SỰ CHÁY I. Thành phần của không khí. - Không khí là hỗn hợp nhiều chất khí. - Thành phần theo thể tích của không khí là: + 21% khí O2 . +78% khí N2 . +1% các khí khác. -Không khí còn chứa cacbonnic (CO2) , hidro (H2), hơi nước (H2O)... * Bảo vệ không khí trong lành, tránh ô nhiễm: pg. 1 Giáo Viên: Lê Duy Minh -Hạ nhiệt độ của chất cháy xuống dưới nhiệt độ cháy. VD: Dùng nước để làm giảm nhiệt độ cháy. -Cách li chất cháy với oxi. VD: Ta dùng bình chữa cháy, hoặc dùng mảnh vài đã thấm nước vào đám cháy để cách ly với oxi. BÀI LUYỆN TẬP 5 I. Kiến thức cần nhớ. 1. Oxi - Tính chất vật lí: Oxi là chất khí không màu, không mùi, ít tan trong nước và nặng hơn không khí. - Tính chất hóa học: + Tác dụng với kim loại: t0 2Cu + O2 2 CuO + Tác dụng với phi kim: t0 S + O2 SO2 + Tác dụng với hợp chất: t0 CH4 + 2O2 CO2 + 2H2O 2. Các khái niệm - Điều chế oxi trong phòng thí nghiệm, người ta điều chế khí oxi bằng cách đun nóng những hợp chất giàu oxi và dễ phân hủy ở nhiệt độ cao. - Sự oxi hoá là sự tác dụng của oxi với một chất ( có thể là đơn chất hoặc hợp chất) pg. 3 Giáo Viên: Lê Duy Minh Bài 2. Những biện pháp phải thực hiện để dập tắt sự cháy là gì ? Tại sao nếu thực hiện được các biện pháp ấy thì sẽ dập tắt được sự cháy ? Hướng dẫn bài 2: Biện pháp dập tắt sự cháy : + Hạ nhiệt độ của chất cháy xuống dưới nhiệt độ cháy ; + Cách li chất cháy với oxi Khi thực hiện được các biện pháp trên sẽ dập tắt được sự cháy vì khi đó điều kiện để sự cháy diễn ra đã không còn và dĩ nhiên sự cháy không thể tiếp tục được nữa. Bài 3. Các oxit sau đây thuộc loại oxit axit hay oxit bazơ ? Vì sao ? Na2O, MgO, CO2, Fe2O3, SO2, P2O5 Gọi tên các oxit đó. Đáp án bài 3: + Oxit axit : CO2 (cacbon đioxit), SO2 (lưu huỳnh đioxit), P2O5 (điphotpho pentaoxit). Vì các oxit của phi kim và có những axit tương ứng. + Oxit bazơ : Na2O ( natri oxit),MgO(magie oxit), Fe2O3 (sắt III oxit). Vì các oxit là các oxit của kim loại và có những bazơ tương ứng. Bài 4. Khoanh tròn ở đầu những câu phát biểu đúng : Oxit là hợp chất của oxi với : a. Một nguyên tố kim loại ; pg. 5 Giáo Viên: Lê Duy Minh 푡0 a) 2KMnO4 K2MnO4 + MnO2 + O2 b) CaO + CO2 → CaCO3 c) 2HgO → 2Hg + O2 푡0 d) Cu(OH)2 CuO + H2O Bài giải: a) Phản ứng phân hủy vì từ một chất KMnO4 phân hủy thành ba chất khác nhau. b) Phản ứng hóa hợp vì từ hai chất CaO và CO2 tạo thành sản phẩm duy nhất CaCO3. c) Phản ứng phân hủy vì từ một chất đầu tiên HgO sinh ra hai chất sau phản ứng. d) Phản ứng phân hủy vì từ Cu(OH)2 phân hủy thành hai chất CuO và nước. Bài 7:Chỉ ra những phản ứng hóa học có xảy ra sự oxi hóa trong các phản ứng cho dưới đây : a. H2 + O2 →2H2O b. 2Cu + O2 → 2CuO c. H2O + CaO → Ca(OH)2 d. 3H2O + P2O5 → 2H2PO4 Bài giải: Các phản ứng oxi hóa là phản ứng a và b. pg. 7 Giáo Viên: Lê Duy Minh Khối lượng Kali clorat (KClO3) cần dùng là : 퐾 푙 3= n . M = 0,066 . (39+35,5+16.3)=8,09 (g) -------Hết------- pg. 9
File đính kèm:
 giao_an_on_tap_hoa_hoc_lop_8_tuan_22_bai_28_khong_khi_su_cha.docx
giao_an_on_tap_hoa_hoc_lop_8_tuan_22_bai_28_khong_khi_su_cha.docx